09/02/2023
Enterokoki, niegdyś znane jako paciorkowce grupy D, to bakterie, które stały się jednym z najgroźniejszych wyzwań współczesnej medycyny. Ich niezwykła zdolność do przetrwania w trudnych warunkach oraz do rozwijania oporności na antybiotyki sprawia, że są one przyczyną poważnych, często śmiertelnych zakażeń, zwłaszcza w środowiskach szpitalnych. Zrozumienie, dlaczego i w jaki sposób te mikroorganizmy stają się niewrażliwe na leki, jest kluczowe dla opracowania skutecznych strategii terapeutycznych i zapobiegania dalszemu rozprzestrzenianiu się oporności.
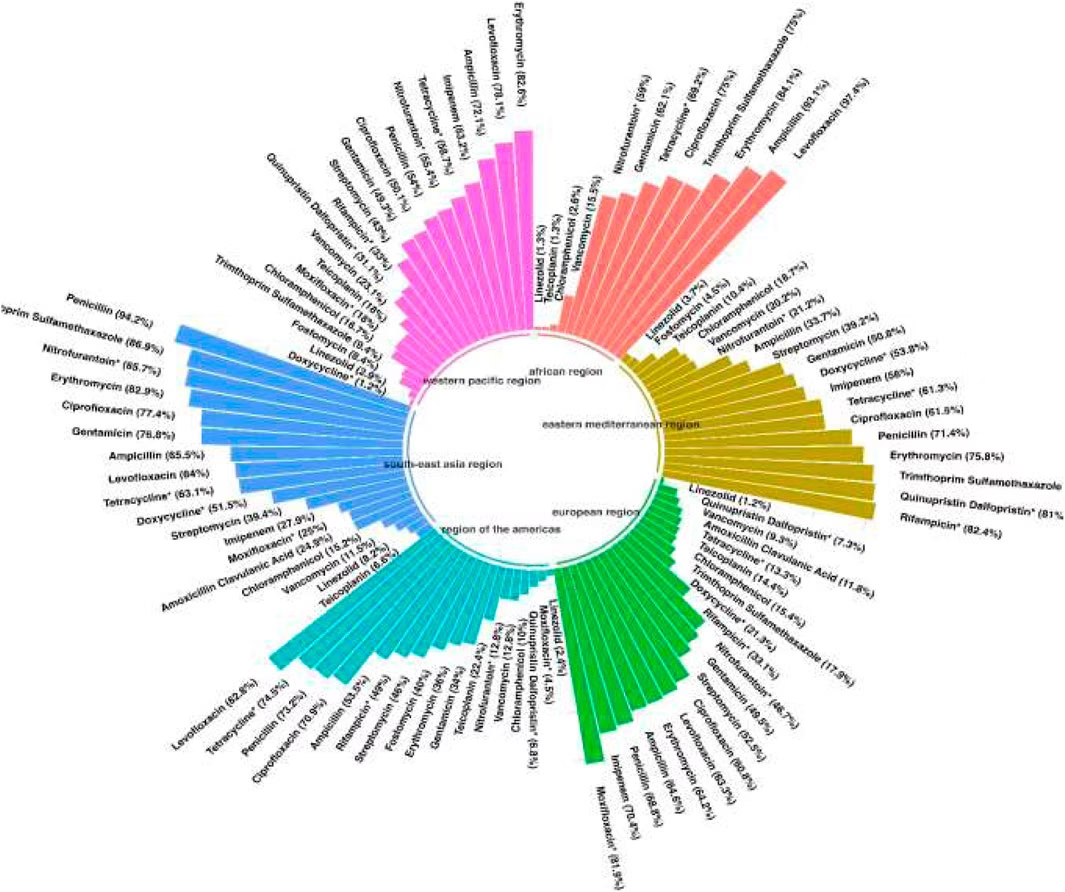
Już od samego początku, Enterokoki były wyposażone w szereg naturalnie występujących (wrodzonych) mechanizmów oporności na antybiotyki. Co więcej, mają one wyjątkową zdolność do nabywania nowych genów oporności i/lub mutacji, co czyni je niezwykle plastycznymi i trudnymi do zwalczenia patogenami. To właśnie ta podwójna natura – wrodzona i nabyta oporność – czyni je tak poważnym zagrożeniem w dzisiejszej opiece zdrowotnej.
Czym są Enterokoki i dlaczego są tak groźne?
Enterokoki to Gram-dodatnie ziarniaki, należące do rodzaju Enterococcus, będącego częścią grupy bakterii mlekowych. Są to fakultatywne beztlenowce, co oznacza, że mogą przetrwać zarówno w warunkach tlenowych, jak i beztlenowych. Powszechnie występują w przewodach pokarmowych ludzi i zwierząt, gdzie zazwyczaj pełnią rolę komensali. Chociaż wiele gatunków Enterococcus jest nieszkodliwych, a nawet korzystnych dla swoich gospodarzy, niektóre gatunki, w szczególności Enterococcus faecalis i Enterococcus faecium, zyskały uznanie jako patogeny oportunistyczne, zdolne do wywoływania szeregu infekcji u ludzi.
Ich znaczenie kliniczne jest ogromne, zwłaszcza w placówkach opieki zdrowotnej. Enterokoki są jednymi z głównych przyczyn zakażeń związanych z opieką zdrowotną (hospitalne zakażenia), w tym zakażeń dróg moczowych (ZUM), zakażeń krwi (BSI), zakażeń miejsca operowanego (SSI) oraz zapalenia wsierdzia. Zakażenia enterokokowe wiążą się z wydłużonym czasem hospitalizacji, zwiększonymi kosztami opieki zdrowotnej i wyższą śmiertelnością, szczególnie wśród pacjentów z obniżoną odpornością i chorobami współistniejącymi.
Rozprzestrzenianie się opornych na antybiotyki szczepów Enterokoków w placówkach opieki zdrowotnej stanowi poważne zagrożenie dla zdrowia publicznego. Organizmy te mogą służyć jako rezerwuary genów oporności, które mogą być przekazywane innym bakteriom, jeszcze bardziej pogłębiając problem antybiotykooporności. Dodatkowo, obciążenie ekonomiczne związane z zakażeniami enterokokowymi, w tym koszty opieki zdrowotnej i straty produktywności, podkreśla znaczenie wdrażania skutecznych strategii zwalczania lekoopornych szczepów Enterococcus.
Dlaczego Enterokoki są naturalnie oporne na antybiotyki?
Jednym z najbardziej niepokojących aspektów bakterii Enterococcus jest ich skłonność do rozwijania oporności na wiele antybiotyków. Oporność ta może być wrodzona, co oznacza, że jest naturalnie obecna w danym gatunku bakterii, lub nabyta poprzez horyzontalny transfer genów od innych bakterii lub spontaniczne mutacje. Enterokoki są znane ze swojej zdolności do nabywania i rozprzestrzeniania genów oporności, co prowadzi do pojawienia się szczepów wielolekoopornych (MDR). Szczególnie niepokojące jest pojawienie się enterokoków opornych na wankomycynę (VRE), co stanowi poważne wyzwanie w leczeniu zakażeń enterokokowych.
Enterokoki, ukształtowane przez selektywne naciski swojego konkurencyjnego środowiska, wyewoluowały różnorodne odpowiedzi i plastyczność genetyczną, pozwalające im prosperować w nowoczesnym środowisku opieki zdrowotnej. Postępy w nowoczesnej medycynie zwiększyły zdolność do podtrzymywania życia u pacjentów krytycznie chorych, zwiększając podatność na infekcje i skutkując szybką rotacją pacjentów oraz powszechnym stosowaniem antybiotyków. Uzbrojone w liczne determinanty oporności na antybiotyki, enterokoki 'wykorzystują' tę okazję i rozprzestrzeniają się w swojej niszy ekologicznej (przewód pokarmowy hospitalizowanych pacjentów), aby zyskać przewagę i zdominować mikroflorę jelitową. Z przewodu pokarmowego, wielolekooporne (MDR) enterokoki szybko rozprzestrzeniają się w środowisku szpitalnym. Rzeczywiście, enterokoki są głównymi przyczynami zakażeń szpitalnych i ustępują jedynie gronkowcom jako przyczynie Gram-dodatnich zakażeń szpitalnych.

Mechanizmy Oporności na Antybiotyki u Enterokoków
Enterokoki rozwinęły szeroki wachlarz mechanizmów oporności na antybiotyki, w tym modyfikację celów leków, inaktywację środków terapeutycznych, nadmierną ekspresję pomp wyrzutowych oraz wyrafinowaną adaptacyjną odpowiedź otoczki komórkowej, która sprzyja przetrwaniu w ludzkim gospodarzu i środowisku szpitalnym. Zrozumienie tych mechanizmów molekularnych jest kluczowe dla opracowania innowacyjnych strategii walki z tymi odpornymi mikroorganizmami.
Oporność na Beta-laktamy (Penicyliny i Cefalosporyny)
Ampicylina i penicylina są najbardziej aktywnymi beta-laktamami przeciwko enterokokom, hamującymi syntezę peptydoglikanu, podstawowej struktury ściany komórkowej bakterii i krytycznego komponentu niezbędnego do przeżycia bakterii. Białka wiążące penicylinę (PBP) to 'konie robocze' maszynerii syntezy ściany komórkowej. Wszystkie enterokoki produkują co najmniej pięć PBP.
- Wrodzona tolerancja i PBP5: Wrodzona tolerancja na działanie beta-laktamów jest związana z obecnością gatunkowo specyficznego genu chromosomowego, pbp5, który koduje białko wiążące penicylinę (PBP) klasy B o niskim powinowactwie do ampicyliny i cefalosporyn. W E. faecium wysoki poziom oporności na ampicylinę (MIC ≥ 128 μg/ml) był początkowo kojarzony ze zwiększoną produkcją tego enzymu, wymagającą wyższego stężenia antybiotyku do nasycenia miejsca aktywnego. Jednakże, wiele opornych izolatów klinicznych nie wykazywało różnic w ekspresji białka, co wskazywało, że oporność w tych szczepach była przypisywana mutacjom zmieniającym sekwencję białka, w szczególności podstawieniu Met485 → Ala w pobliżu aktywnej reszty serynowej oraz insercji reszty serynowej w pozycji 466. Te zmiany zmniejszają wiązanie beta-laktamów i zwiększają MIC.
- Beta-laktamazy: Inna forma oporności na ampicylinę jest pośredniczona przez enzym beta-laktamazę, która inaktywuje antybiotyk poprzez rozszczepienie pierścienia beta-laktamowego. Gen blaZ, pierwotnie opisany u gronkowców, koduje tę beta-laktamazę jako część operonu. W przeciwieństwie do gronkowców, blaZ w enterokokach jest wyrażany konstytutywnie, ale na znacznie niższym poziomie, co skutkuje klinicznie istotnym efektem inokulum. Oznacza to, że przy standardowych stężeniach bakterii w testach wrażliwości (zazwyczaj 1 × 105 organizmów na ml) enterokoki produkują tak mało enzymu, że wydają się wrażliwe, podczas gdy przy wysokim inokulum, takim jak podczas infekcji, obecność większej ilości enzymu prowadzi do oporności. Po zidentyfikowaniu, obecność beta-laktamazy nie stanowi poważnego problemu klinicznego, ponieważ dodatek inhibitora beta-laktamazy, takiego jak sulbaktam (np. ampicylina-sulbaktam), jest wystarczający do przywrócenia skuteczności antybiotyku.
- L,d-transpeptydaza (Ldtfm): Rozwój oporności na ampicylinę poprzez l,d-transpeptydazę znaną jako Ldtfm również został opisany in vitro. Enzym ten, konstytutywnie wyrażany w E. faecium, wykorzystuje substrat tetrapeptydowy (w przeciwieństwie do d,d-transpeptydaz, które działają na pentapeptydy) i uważa się, że bierze udział w utrzymaniu peptydoglikanu w fazie stacjonarnej. Mutacje w ukrytym locus (ddc), kodującym domniemany dwuskładnikowy system transdukcji sygnału (TCS), indukowały ekspresję d,d-karboksy peptydazy (DdcY), która dzieli podobieństwa z klastrem oporności van i produkowała niezbędny substrat tetrapeptydowy. Ten szlak może umożliwić syntezę funkcjonalnej ściany komórkowej w obecności glikopeptydów.
Oporność na Cefalosporyny
Chociaż naturalna oporność enterokoków na cefalosporyny jest dobrze znaną cechą, molekularne podstawy tego fenotypu nie są w pełni poznane. Częstą obserwacją jest to, że wrodzona oporność jest związana ze zmniejszeniem powinowactwa wiązania cefalosporyn do enterokokowych PBP, w szczególności Pbp5. Jako PBP klasy B posiadające tylko aktywność transpeptydazy, Pbp5 musi współpracować z glikozylotransferazą, aby syntetyzować peptydoglikan. Badania wykazały, że PonA lub PbpF są potrzebne do ekspresji oporności na cefalosporyny. Usunięcie wszystkich trzech genów (PbpF, PonA, PbpZ) prowadziło do fenotypu wrażliwego, choć potrójny mutant był nadal żywotny, aczkolwiek z upośledzoną szybkością wzrostu.
Ponadto, kilka szlaków regulacyjnych kontrolowanych przez bakteryjne dwuskładnikowe systemy regulacyjne (TCS) również zostało powiązanych z wrodzoną opornością na cefalosporyny. Wśród nich, CroRS okazał się ważny dla oporności na cefalosporyny. Inny TCS zaangażowany w oporność składa się z kinazy serynowo-treoninowej zwanej IreK i fosfatazy IreP. System ten wydaje się być specyficzny dla oporności na cefalosporyny, ponieważ MIC dla ampicyliny i innych środków aktywnych na ścianę komórkową pozostały niezmienione. Jednym z białek, które mogą być zaangażowane w efekty sygnalizacyjne szlaku IreK, jest MurAA, jeden z pary homologów, które katalizują pierwszy etap syntezy peptydoglikanu.
Oporność na Glikopeptydy (Wankomycyna)
Glikopeptydy (wankomycyna i teikoplanina) wiążą się z końcową resztą d-alaniny-d-alaniny (d-Ala-d-Ala) prekursorów peptydoglikanu, zapobiegając w ten sposób sieciowaniu łańcuchów peptydoglikanu i hamując syntezę ściany komórkowej. Oporność na te środki, typowa dla wankomycyny, może być opisana jako wysoki poziom (MIC > 64 μg/ml) lub niski poziom (MIC od 4 do 32 μg/ml), oba wynikające ze zmiany końcowych aminokwasów prekursora peptydoglikanu z d-Ala-d-Ala na d-alaninę-d-mleczan (d-Ala-d-Lac) lub, rzadziej, d-alaninę-d-serynę (d-Ala-d-Ser). Zmiana typu aminokwasu jest istotna, ponieważ określa poziom oporności. Niski poziom oporności jest nadawany przez prekursory zakończone d-Ala-d-Ser, co zmniejsza powinowactwo wiązania antybiotyku około siedmiokrotnie. Z drugiej strony, wysoki poziom oporności opiera się na zmianie końcowego pentapeptydu na d-Ala-d-Lac, podstawienie, które eliminuje jedno z pięciu wiązań wodorowych wymaganych do wiązania wankomycyny z łańcuchem peptydoglikanu, zmniejszając jej powinowactwo około 1000-krotnie.
Pochodzenie klastrów genów oporności na wankomycynę (oznaczonych jako van) prawdopodobnie leży w codziennej walce o przetrwanie w świecie mikrobowym. Geny niemal identyczne z klastrem vanA znalezionym w enterokokach zostały opisane u bakterii glebowych Paenibacillus thiaminoluticus i P. apiaries. Do tej pory opisano dziewięć różnych klastrów oporności na wankomycynę w enterokokach (vanA, vanB, vanC, vanD, vanE, vanG, vanL, vanM i vanN). Ogólnie rzecz biorąc, klastry te składają się z trzech grup genów kodujących: dwuskładnikowe systemy regulacyjne (TCS); enzymy niezbędne do syntezy nowych prekursorów peptydoglikanu oraz enzymy niszczące normalne prekursory kończące się na d-Ala-d-Ala. Różne klastry można odróżnić na podstawie tożsamości na poziomie aminokwasów enzymu ligazy (np. VanA vs VanB), stopnia nadanej oporności na wankomycynę, zdolności systemu do indukcji po ekspozycji na teikoplaninę oraz strukturalnego układu klastra genów.
- vanA: Jest najczęstszym mediatorem oporności na wankomycynę w enterokokach, a jego ekspresja jest regulowana przez dwa promotory. Pierwszy jest odpowiedzialny za transkrypcję VanRS, systemu TCS, który reguluje ekspresję i funkcję VanA. Sensorem systemu jest VanS, transbłonowe białko z domeną kinazy histydynowej, które reaguje na obecność glikopeptydów poprzez fosforylację regulatora odpowiedzi VanR. Po aktywacji VanR wiąże się z drugim regionem promotora, położonym powyżej genów oporności, aktywując ich transkrypcję. VanH produkuje d-mleczan z pirogronianu. Następny gen, vanA, produkuje ligazę, która umożliwia dodanie d-Lac do d-Ala przed dodaniem go do prekursora trypeptydowego. Powstały pentadepsipeptyd jest włączany do rosnącej ściany komórkowej i umożliwia sieciowanie struktury peptydoglikanu. VanX, d,d-dipeptydaza, i VanY, DdcY, działają w celu usunięcia typowych dipeptydów d-Ala-d-Ala (które wiązałyby wankomycynę, gdyby były włączone do ściany komórkowej) i normalnych łańcuchów pentapeptydowych zakończonych d-Ala z puli prekursorów ściany komórkowej.
- vanB: Jest również powszechnie spotykany w klinicznych izolatach enterokoków i funkcjonuje w podobny sposób do klastra VanA, z kilkoma ważnymi różnicami. Kinaza sensorowa (VanSB) i regulator odpowiedzi (VanRB) mają tylko odległy związek (34% i 23% tożsamości sekwencji, odpowiednio) ze swoimi homologami VanA. W związku z tym VanSB nie jest aktywowany w obecności teikoplaniny, co pozwala szczepom z fenotypem VanB pozostać wrażliwymi na ten antybiotyk. Co ważne, oporność na teikoplaninę może wynikać z mutacji w kinazie sensorowej, umożliwiających aktywację systemu w obecności antybiotyku lub upośledzenia zdolności regulacyjnej fosfatazy VanSB, co skutkuje konstytutywną ekspresją genów oporności. VanB również nie posiada genu vanZ, a zamiast tego posiada vanW, którego funkcja jest również nieznana.
- vanC: Jest wrodzoną cechą dwóch gatunków enterokoków, Enterococcus gallinarum i Enterococcus casseliflavus. Jest to chromosomowo kodowany klaster genów, który (wraz z innymi genami) nadaje niski poziom oporności na wankomycynę poprzez zmianę końcowego dipeptydu z d-Ala-d-Ala na d-Ala-d-Ser. Gatunki te produkują zmieniony dipeptyd d-Ala-d-Ser za pośrednictwem VanT, racemazy serynowej, która katalizuje zmianę z l-Ser na d-Ser. Ponadto, posiadają również bifunkcyjną d,d-peptydazę/DdcY, oznaczoną jako VanXYC, która hydrolizuje typowe prekursory d-Ala-d-Ala w cytoplazmie.
- vanD: Enterokoki ekspresjonujące VanD nie posiadają aktywnego sygnałowego TCS z powodu inaktywującej mutacji VanSD lub VanRD. W rezultacie oporny fenotyp jest konstytutywnie wyrażany poprzez stałą aktywację operonu, produkującego depsipeptyd d-Ala-d-Lac. Spodziewano by się, że obciążyłoby to bakterie znacznym obciążeniem metabolicznym, ponieważ konieczne jest utrzymanie jałowego cyklu syntezy i niszczenia d-Ala-d-Ala, pomimo braku zagrożenia glikopeptydami. Jednakże, szczepy te posiadają również drugą mutację w genie ddl, kodującym ligazę odpowiedzialną za produkcję normalnych prekursorów peptydoglikanu. W rezultacie wyrażają one fenotyp oporności bez znacznego zmniejszenia sprawności.
- vanE: Podobnie jak VanC, jest chromosomowo kodowany, wyraża niski poziom oporności i jest pod kontrolą pojedynczego promotora. Co ciekawe, funkcjonalny fenotyp oporności VanE był w pełni wyrażany pomimo inaktywacji VanSE przez przedwczesny kodon stop. Zaproponowano aktywację i transkrypcję operonu przez nieokreślony endogenny TCS, co podkreśla solidną naturę odpowiedzi enterokoków na stres.
Tabela Porównawcza Typów Oporności na Wankomycynę
Poniższa tabela przedstawia kluczowe różnice między najczęściej spotykanymi typami oporności na wankomycynę u enterokoków:
| Typ Oporności | Poziom Oporności | Zmieniony Prekursor | Indukcja Teikoplaniną | Występowanie | Uwagi |
|---|---|---|---|---|---|
| VanA | Wysoki (MIC > 64 μg/ml) | d-Ala-d-Lac | Tak | Wiele gatunków Enterococcus (najczęściej E. faecium) | Najczęstszy i najbardziej problematyczny typ. |
| VanB | Wysoki (MIC > 64 μg/ml) | d-Ala-d-Lac | Nie | Wiele gatunków Enterococcus (często E. faecalis) | Szczepy pozostają wrażliwe na teikoplaninę. |
| VanC | Niski (MIC 4-32 μg/ml) | d-Ala-d-Ser | Nie (wrodzona) | E. gallinarum, E. casseliflavus (wrodzona) | Chromosomowo kodowana, naturalna oporność. |
| VanD | Wysoki (MIC > 64 μg/ml) | d-Ala-d-Lac | Konstytutywna | Rzadziej spotykany | Nieaktywny system TCS, oporność wyrażana stale. |
| VanE | Niski (MIC 4-32 μg/ml) | d-Ala-d-Ser | Tak | Rzadziej spotykany | Chromosomowo kodowana, niski poziom oporności. |
Wyzwania i Strategie Walki z Opornością
Pomimo dostępności nowszych środków przeciwko bakteriom Gram-dodatnim (np. linezolid, chinuprystyna/dalfoprystyna [Q/D], daptomycyna [DAP], tygecyklina), enterokoki szybko się przystosowały, a pojawienie się oporności na wszystkie te nowsze środki zostało dobrze udokumentowane. To zjawisko sprawia, że leczenie zakażeń enterokokowych MDR jest niezwykle trudnym wyzwaniem klinicznym. Systemy genów kodujących TCS klastrów genów van są eleganckim systemem, który pozwala bakteriom zrównoważyć potrzebę oporności na antybiotyki i koszt, jaki ponoszą dla komórki.
Rozwiązanie problemu oporności Enterokoków na leki ma ogromne znaczenie z kilku powodów. Po pierwsze, zakażenia Enterokokami, zwłaszcza te spowodowane przez szczepy wielolekooporne, wiążą się ze zwiększoną zachorowalnością i śmiertelnością. Infekcje te mogą być trudne do leczenia ze względu na ograniczone możliwości terapeutyczne, prowadząc do niepowodzeń leczenia i niekorzystnych wyników dla pacjentów. Po drugie, rozprzestrzenianie się opornych na antybiotyki szczepów Enterokoków w placówkach opieki zdrowotnej stanowi poważne zagrożenie dla zdrowia publicznego. W związku z tym, istnieje pilna potrzeba opracowania nowych celów leków i terapii skojarzonych przeciwko tym wytrzymałym i trudnym do zwalczenia organizmom. Tylko gruntowne zrozumienie mechanizmów leżących u podstaw oporności na antybiotyki u enterokoków jest pierwszym krokiem do opracowania strategii kontroli rozprzestrzeniania się tych organizmów i potencjalnego ustanowienia nowatorskich podejść terapeutycznych.
Często Zadawane Pytania (FAQ)
- Czy wszystkie Enterokoki są oporne na antybiotyki?
Nie, nie wszystkie Enterokoki są oporne na antybiotyki. Jednakże, Enterokoki posiadają wrodzoną tolerancję na wiele antybiotyków, a także wyjątkową zdolność do nabywania nowych genów oporności, co sprawia, że szczepy wielolekooporne są coraz powszechniejsze, zwłaszcza w środowisku szpitalnym.
- Co to jest VRE i dlaczego jest tak niebezpieczne?
VRE to skrót od Vancomycin-Resistant Enterococcus, czyli Enterokoki oporne na wankomycynę. Są one szczególnie niebezpieczne, ponieważ wankomycyna jest często lekiem ostatniej szansy w leczeniu poważnych infekcji Gram-dodatnich. Oporność na ten antybiotyk znacznie ogranicza opcje terapeutyczne, prowadząc do trudniejszych do leczenia, a często śmiertelnych infekcji.
- Jak Enterokoki nabywają oporność?
Enterokoki nabywają oporność na kilka sposobów: poprzez spontaniczne mutacje w ich własnym materiale genetycznym, a także poprzez horyzontalny transfer genów, czyli wymianę genów oporności z innymi bakteriami. Są to bardzo plastyczne genetycznie organizmy, co pozwala im szybko adaptować się do presji selekcyjnej wywieranej przez antybiotyki.
- Czy można zapobiegać rozprzestrzenianiu się opornych Enterokoków?
Tak, kluczowe jest przestrzeganie ścisłych zasad higieny w placówkach medycznych, racjonalne stosowanie antybiotyków (aby ograniczyć presję selekcyjną) oraz wczesne wykrywanie i izolowanie pacjentów zakażonych szczepami opornymi. Rozwój nowych leków i terapii skojarzonych również stanowi ważny kierunek działań.
Zainteresował Cię artykuł Oporność Enterokoków na Antybiotyki: Głębsze Spojrzenie? Zajrzyj też do kategorii Kulinaria, znajdziesz tam więcej podobnych treści!

